糖化应激和抗衰老
糖化应激和AGEs受体
糖化应激和AGEs受体
随着糖化应激的增强,当AGEs在血中和组织中形成并蓄积,生理功能的下降和障碍会进展。近年来,了解了AGEs通过受体在细胞内传递信号的途径,并明确了捕获和清除AGEs的受体是存在的(图1)(1)。
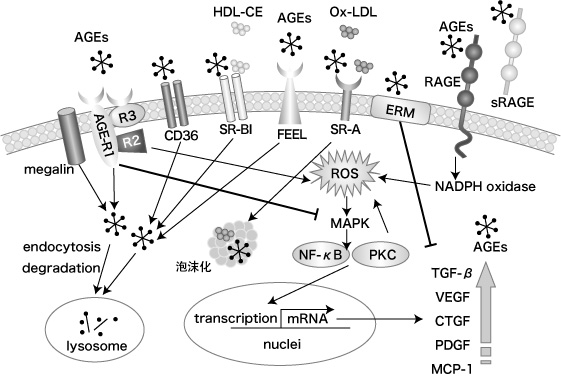 图1 AGEs受体
图1 AGEs受体
深水圭等(2013)(1)
AGEs的受体可大致分为(1)与炎症有关的受体,(2)与AGEs的分解和清除有关的受体。 (1)中包括receptor for AGEs(RAGE)、AGE-R2。 (2)中包括AGE-R1、AGE-R3、CD36、SR-A、SR-BI、FEEL-1,2、ERM和巨蛋白。这些受体在血管、肾脏、神经、巨噬细胞、造血干细胞中表达(表1)(1)。本文总结了典型的AGEs受体及其功能。
| AGEs受体 | 大小 | 配体 | 主要功能 | 表达部位 |
|---|---|---|---|---|
| RAGE | 45 | AGEs, HMGB1, β-amyloid, S100/calgranulins | 动脉硬化、糖尿病并发症、促进炎症 | 单核细胞、巨噬细胞 神经和肾脏、血管平滑肌细胞、内皮细胞 |
| AGE-R1 (OST-48) |
48 | AGEs | 清除AGEs、降低氧化应激 | 内皮细胞、系膜细胞、巨噬细胞、单个核细胞 |
| AGE-R2 (80K-H) |
80 | None | 激活细胞内信号 | 单个核细胞、肾脏、内皮、脑、神经 |
| AGE-R3 (galectlin3) |
32 | AGEs | 清除AGEs、抑制细胞增殖和凋亡 | 巨噬细胞、嗜酸性粒细胞、肥大细胞、消化器官和呼吸器官的黏膜、神经、肾脏 |
| SR-A | 220~250 | AGEs、Ac-LDL Ox-LDL |
促进动脉硬化、肾病、泡沫细胞化 | 单个核细胞、巨噬细胞 |
| CD36 | 88 | AGEs, Ox-LDL | 清除AGEs | 巨噬细胞、血管内皮细胞、脂肪细胞 |
| SR-BI | 57 | AGEs, HDL, Ac-LDL, Ox-LDL |
分解AGEs、抽取HDL的CE | 巨噬细胞、肝脏、肾上腺、卵巢、睾丸、胎盘 |
| FEEL1,2 | AGEs、细菌、LDL | 细胞、修饰LDL、AGEs的细胞内掺入、分解 | 脾脏、淋巴结、单个核细胞、内皮细胞 | |
| ezrin, radixin, moesin (ERM) | AGEs, 各种低分子量蛋白 |
细胞的结构变化、细胞的运动、粘附 | 近端小管细胞 | |
| megalin | 600 | AGEs, 各种低分子量蛋白 |
清除AGEs | 近端小管细胞 |
表1 AGEs受体和功能
深水圭等(2013)(1)
RAGE
RAGE从属于分子量为45kDa的免疫球蛋白超家族,是一种单跨膜型的膜蛋白,在单核细胞、巨噬细胞、神经、肾小管细胞、系膜细胞等中表达。 除AGEs外,RAGE还可与β-淀粉样蛋白、S100/calgranulins和high mobility group box 1(HMGB-1)结合,并参与炎症和氧化应激的增强。
RAGE由存在于细胞外的V结构域和两个C结构域、跨膜结构域、胞内结构域这5个结构域组成(图2)。
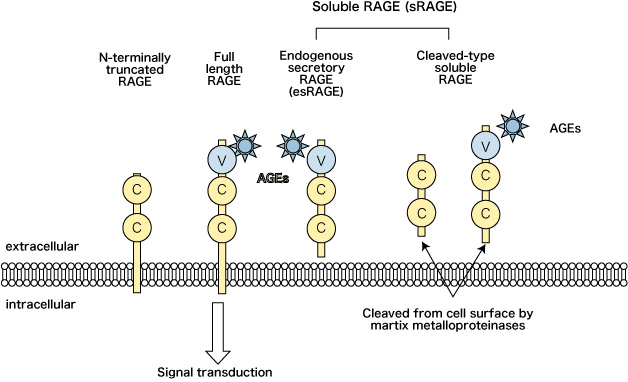
图2 RAGE及其变异体
RAGE = receptor for advanced glycation end-products;
sRAGE = soluble form of RAGE;
esRAGE = endogenous secretory RAGE;
C = immunoglobulin-like constant domains;
V = immunoglobulin-like variable domains
Katakami N, et al. (2007)(12)
此外,RAGE中除存在于细胞表面的全长型(full length RAGE:F-RAGE)外,还存在作为剪接变异体(splicing variant)的胞内结构域缺失型(C-terminally truncated RAGE:C-RAGE)和胞外V结构域缺失型(N-terminally truncated RAGE:N-RAGE)(3)。
其中,胞内结构域缺失型RAGE被称为可溶性RAGE(soluble RAGE:sRAGE)。而sRAGE存在在胞内产生并分泌到胞外的endgenous secretory RAGE(esRAGE),以及F-RAGE被蛋白水解酶和matrix metalloproteinases(MMP)的a disintegrin and metalloproteinase 10(ADAM 10)切断并释放到血液中的cleaved-type soluble RAGE(CL-RAGE)(4)。
当F-RAGE在细胞膜上与AGEs结合时,NADPH氧化酶被激活,细胞内氧化应激增强,并通过激活NF-kB,诱导各种细胞因子、生长因子的分泌和粘附分子的表达上调(5)。此外,可认为氧化应激增强使一氧化氮(NO)失活,进一步加剧炎症反应和血栓的形成趋势,并参与动脉硬化的进展。
而且,AGEs促进血管内皮细胞中血管内皮生长因子(VEGF)的自分泌产生,诱导血管生成(6)。
另外,F-RAGE与AGEs的结合会抑制血管内皮细胞中前列环素(PGI2)的产生,同时促进纤溶酶原激活物抑制物-1(PAI-1)的合成,并抑制纤溶活性,影响血栓的稳定(7)。 已知AGEs会在增强血小板聚集的同时,促进凝血级联。
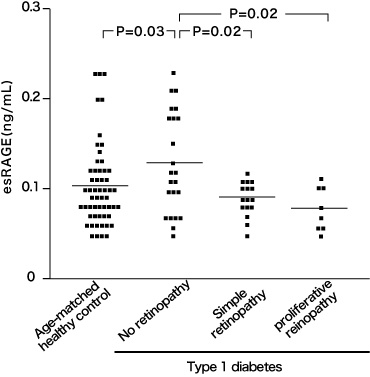
另一方面,由于sRAGE具有与AGEs结合的位点,因此可认为其会诱捕存在于细胞外的AGEs,作为抑制与存在于细胞表面的RAGE结合的诱骗受体发挥作用(8)。 2型糖尿病患者的血esRAGE显著性低于非糖尿病患者,表明其可能与2型糖尿病患者的发病有关(9-10)。另有报告显示,在1型糖尿病患者血esRAGE水平较低的病例中,视网膜病变的发病风险较高(图3)(11)。而且,还显示了2型糖尿病患者的血esRAGE水平,与颈动脉硬化、冠状动脉疾病的严重程度呈负相关(12-13)。
图3 1型糖尿病患者的血清esRAGE
与视网膜病变的关系
水平线表示各组的平均值;Scheffe´s F-test.
Sakurai S, et al. (2006)(11)
AGE-R1、-R2、-R3复合物
AGE-R1也被称为OST-48(oligosaccharyltransferase-48),从属于分子量为48kDa的凝集素家族,是一种单跨膜型蛋白。 AGE-R1在内皮细胞、系膜细胞、巨噬细胞等中表达,通过内吞作用(endocytosis)清除AGEs。此外,AGE-R1可能与寿命延长有关(14)。
AGE-R2也被称为80K-H(80kDa protein kinase C substrate),是一种分子量为80kDa的酪氨酸磷酸化蛋白质,存在于细胞质中。 AGE-R2在单个核细胞、肾脏、血管内皮、脑、神经等中表达,参与细胞内信号的激活。
AGE-R3也被称为galectin-3,是一种属于分子量为32kDa的凝集素家族的受体。 AGE-R3通过细胞上的碳水化合物识别结构域,并与AGEs直接结合,在巨噬细胞、嗜酸性粒细胞、肥大细胞、神经、肾脏等中表达。 AGE-R3的作用包括:细胞与作为基质的层粘连蛋白(laminin)的粘附抑制、肥大细胞的激活、细胞生长和凋亡的调控、以及通过内吞作用分解AGEs等。此外,AGE-R3的表达在年龄增长和糖尿病时上调,因此对衰老可能具有保护作用(15)。
SR-A, CD36, SR-BI, FEEL-1, FEEL-2
SR-A、CD36、SR-BI、FEEL-1、FEEL-2也被称为清道夫受体,对AGEs的分解排泄起作用。
SR-A(scavenger receptor class A)将乙酰化LDL(low density lipoprotein)和氧化LDL识别为配体,在巨噬细胞的细胞表面将AGEs掺入到细胞内形成泡沫,由此表明其与动脉粥样硬化有关(16)。
CD36(cluster of differentiation 36)在巨噬细胞、血管内皮细胞和脂肪细胞表面表达。 CD36与脂肪酸、胶原蛋白、氧化LDL结合,发挥将氧化LDL掺入巨噬细胞内和将脂肪酸运输到脂肪细胞中的作用。 由于CD36可将AGEs掺入脂肪细胞内分解清除AGEs,因此推测其对动脉硬化具有保护作用(17)。
SR-BI(scavenger receptor-BI)在巨噬细胞、肝脏、肾上腺和卵巢等中表达,具有促进HDL(high density lipoprotein)胆固醇酯向肝脏掺入的作用(18)。
FEEL-1(fasciclin EFG-like laminin-type EGF-like and link domain-containing scavenger receptor-1)、FEEL-2在脾脏、淋巴结中表达,参与AGEs的细胞内掺入和分解(19)。
巨蛋白
巨蛋白(megalin)是分子量约为600kDa的糖蛋白,属于LDL受体基因家族,存在于近端小管细胞中(20)。巨蛋白主要参与低分子量蛋白,如维生素D结合蛋白、视黄醇结合蛋白、甲状腺激素、胰岛素等的重吸收和代谢。近年的报告显示,in vitro实验中证实了巨蛋白会与AGE结合,通过肾小球的AGEs被巨蛋白捕获,并被溶酶体吸收分解(21)。
其他AGEs受体
ERM蛋白(ezrin、radixin、moesin)是一种联结细胞膜和细胞内肌动蛋白丝的蛋白,在细胞的运动、粘附和结构变化等中起作用。近年有报告指出,ERM家族蛋白的N末端会与AGEs结合(22)。
糖化应激抑制和AGEs受体
AGEs与RAGE的结合会增强细胞内的氧化应激,促使细胞因子表达,在细胞内诱发炎症,并引起器官和组织损伤。因此,抑制RAGE的表达是抑制糖化应激的一个靶标。另一方面,AGE-R1和AGE-R3起保护器官和组织的作用。此外,sRAGE诱骗性地作用于AGEs,抑制由RAGE表达引起的炎症,阻止各种疾病的进展。因此认为,清除AGEs的受体和抑制sRAGE的表达,可能在今后成为抑制糖化应激的新手段。
糖化应激和抗衰老
- 什么是糖化应激?
- 糖化应激标志物的检测方法(1) 血糖、糖化蛋白、糖化反应中间体的检测
- 糖化应激标志物的检测方法(2) AGEs的检测
- 糖化应激标志物的检测方法(3) 抗糖化作用评价
- 糖化应激和AGEs受体
- 糖化应激与肾疾病
- 糖化应激和皮肤老化
- 糖化应激与动脉硬化
- 糖化应激和精神分裂症
- 糖化应激与肝病
- 糖化应激与不孕症
- 糖化应激与阿尔兹海默症
- 糖化应激对策(1) 血糖控制
- 糖化应激对策(2) 糖化反应的抑制
- 糖化应激对策(3) AGEs的降解和排泄
- 糖化应激对策(4) 膳食来源的AGEs
- 糖化应激对策的课题和展望